1 概要
臨床試験を適切に評価するためには、完全 (complete),明快 (clear),透明性の高い (transparent) 情報が必要とされていますが、多くの報告者はそれらの重要な情報について明確 (lucid) に完全に記述できているとは言い難いのが現状です。新たな方法論的エビデンスや蓄積された経験の成果として、臨床試験について適切に報告するための指針となるCONSORT2010声明が発表されています。本稿は、臨床試験の報告に携わるすべての方に向けて報告書記述のヒントをまとめます。
2 参加者の流れ (Participant flow)
本稿は、CONSORT2010のチェックリストにある「参加者の流れ (Participant flow)」についてまとめます。
2.1 CONSORT2010声明
CONSORT2010声明には統計学的手法について以下のような記述がなされています。
| Participant flow (a diagram is strongly recommended) |
13a |
For each group, the numbers of participants who were randomly assigned, received intended treatment, and were analysed for the primary outcome |
|---|---|---|
| 13b | For each group, losses and exclusions after randomisation, together with reasons | |
| 参加者の流れ (フローチャートを 強く推奨) |
13a | 各群について, ランダム割付けされた人数, 意図された治療を受けた人数, 主要アウトカムの解析に用いられた人数の記述。 |
| 13b | 各群について, 追跡不能例とランダム化後の除外例を理由とともに記述。 |
2.2 参加者の流れを記述する際の留意点
CONSORT初版からCONSORT2010への改訂点の一つとして、試験参加者の参加状況の流れをフローチャートとして図示することを推奨するようになったという点があります。以下の段階において収集すべき情報が得られている、あるいは得られていない試験参加者の人数を示し、情報が得られていない試験参加者に関してはその理由も明示すべきとされています。
-
- ・組入れ (enrolment)
- スクリーニング検査を受診し、適格性 (eligibility)を評価された試験参加者の人数、その結果プロトコルで定めた選択基準に含まれない、あるいは参加辞退を希望して組み入れ対象から除外された人数、スクリーニングを通過しランダム化の対象となった人数を記述します。
-
- ・割振り (allocation)
- ランダム化の結果、それぞれの群に割り振られた人数を記述します。更に各群の中で、割り振られた介入を受けた人数とともに、介入を受けなかった人数をその理由別に記述します。
-
- ・追跡 (follow-up)
- 試験期間を通して、収集すべき情報が全て入手できなかった人数をその理由別に記述します。
-
- ・解析 (analysis)
- プロトコルで定めた解析データセットの定義に該当するため解析の対象になった人数、定義に抵触するため解析対象から除外された人数をその理由別に記述します。
3 記載例
記載例は以下の通りです。
-
- ・被験者の内訳及び解析対象集団
-
試験参加の同意が得られた●●例のうち、登録除外例●●例を除いた●●例が適格被験者として二次登録された。これら●●例は無作為に割り付けられ、プラセボ群●●例、被験食品群●●例となった。割り付けられた介入を受けなかった試験参加者がプラセボ群に●●例見受けられた。全ての検査段階が終了した後の症例検討会において、プロトコルからの重大な逸脱が確認された症例がプラセボ群に●●例、被験食品群に●●例確認された。介入を受けた被験者のすべてが有効性の主たる解析対象であるFAS及び安全性の解析対象である安全性解析対象集団となった。このうちPPSは●●例(プラセボ群●●例、被験食品群●●例)であった。
試験参加者の参加状況の流れを示すフローチャートの例として、CONSORT2010声明の日本語版に下図が掲載されています。
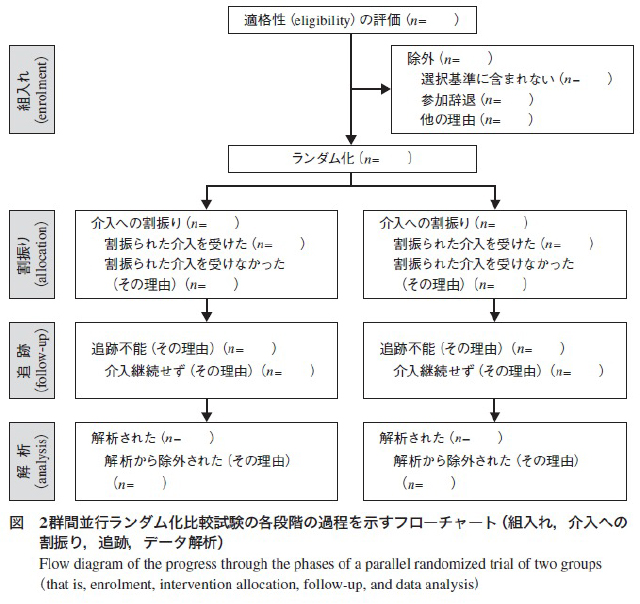
割付後の中止やプロトコルからの逸脱が見られた場合は、その理由を適切に要約して分類する必要があります。
-
- ・中止の理由として用いられる文言
-
- 追跡不能
- 有害事象の発生
- 試験食品摂取遵守の不良 など
-
- ・プロトコルからの逸脱と判断した理由として用いられる文言
-
- 組み入れ基準を満たしていないにもかかわらず治験に組み入れられた
- 治験期間中に中止基準に該当するようになったが,中止されなかった
- 治療方法や用量が不適切であった
- 禁止されている併用療法を受けた など
4 参考文献
- Schulz KF, Altman DG, Moher D; CONSORT Group. CONSORT 2010 statement: updated guidelines for reporting parallel group randomised trials. BMJ. 2010; 340: c332. (PMID: 20332509)
- 津谷 喜一郎, 元雄 良治, 中山 健夫, 訳. CONSORT2010声明 ランダム化並行群間比較試験のための最新版ガイドライン. 薬理と治療. 2010; 939-47: (http://www.consort-statement.org/Media/Default/Downloads/Translations/Japanese_jp/Japanese%20CONSORT%20Statement.pdf) (2021年8月19日アクセス可能)
- 厚生労働省. 治験の総括報告書の構成と内容に関するガイドラインについて (平成8年5月1日). (https://www.pmda.go.jp/files/000156923.pdf) (2021年8月18日アクセス可能)
ヒト臨床試験 (ヒト試験) で得られる結果は、様々な誤差を含んでいます。この誤差を小さくすることで介入効果を増大させることができます。オルトメディコは、多分野の専門家を有するため、様々なアプローチにより誤差を最小化する試験運営が可能です。引き続き、皆様にご満足いただけるような高品質なヒト試験を提供させていただきますので、今後ともどうぞ宜しくお願い申し上げます。
- ★問い合わせ★
-
-
①臨床試験のお見積りに関するお問い合わせ
HP: https://orthomedico.jp/contact.html
Mail: info@orthomedico.jp -
②臨床試験に参加したい方はコチラ
HP: https://www.go106.jp/ -
③機能性表示食品の届け出に関するお問い合わせ
HP: https://届出.com/
Mail: planning-department@orthomedico.jp -
④栄養計算に関するお問い合わせ
HP: https://www.cand.life/
Mail: info@CAND.life -
⑤研究会の開催に関するお問い合わせ
HP: https://はじめての研究会.jp/
Mail: info@hajiken.jp
-
①臨床試験のお見積りに関するお問い合わせ
